Bảng nguyên tố chất hóa học lớp 8 có ý nghĩa sâu sắc vô cùng đặc biệt quan trọng trong chương trình huấn luyện và giảng dạy bộ môn Hóa học. Có không ít nguyên tố không giống nhau trong bảng, từng nguyên tố hoặc đội nguyên tử sẽ có những hóa trị riêng. Cùng tham khảo bài viết dưới đây để hiểu thêm về nguyên tố chất hóa học lớp 8 nhé.
Bạn đang xem: Bảng nguyên tố hoá học
1. Bảng Nguyên Tố hóa học Lớp 8 – Hóa trị của một trong những chất thường xuyên gặp
Bảng nguyên tố hóa học 8 gồm có các thông tin về Số Proton, tên, ký kết hiệu hóa học, nguyên tử khối với hóa trị của nguyên tố gắng thể. Trong bảng sẽ bao hàm 30 nguyên tố chất hóa học thường xuất hiện thêm trong lịch trình học chất hóa học lớp 8. Vậy nguyên tố hóa học lớp 8 là gì? Hóa trị của một số trong những chất thường gặp là bao nhiêu?

Hóa trị của tập thể nhóm nguyên tử trong bảng nguyên tố hóa học lớp 8.
3. Bài ca hóa trị – Mẹo nhớ nhanh hóa trị của các nguyên tố chất hóa học lớp 8
Phần bự học sinh đều thấy khó khăn trong việc ghi lưu giữ hóa trị lúc được học tập về bảng nguyên tố chất hóa học lớp 8. Tuy nhiên, có không ít mẹo nhằm giúp chúng ta học ghi nhớ một cách dễ dàng và đơn giản và dễ hiểu thông qua các bài xích ca hóa trị. Dưới đấy là 1 bài ca hóa trị thông dụng mà các chúng ta cũng có thể tham khảo:
“Kali, Iot, Hidro
Natri cùng với Bạc, Clo một loài
Có hóa trị một chúng ta ơi
Nhớ ghi cho rõ kẻo rồi phân vân
Magie, Chì, Kẽm, Thủy ngân
Canxi, Đồng ấy cùng tương đương Bari
Cuối thuộc thêm chú Oxi
Hóa trị hai ấy có gì nặng nề khăn
Bác Nhôm hóa trị tía lần
Ghi sâu trí tuệ khi cần phải có ngay
Cacbon, Silic này đây
Là hóa trị bốn không ngày như thế nào quên
Sắt kia đề cập cũng thân quen tên
Hai, cha lên xuống thiệt phiền lắm thay
Nitơ băn khoăn nhất đời
Một, hai, ba, tư khi thì là năm
Lưu huỳnh lắm lúc thi đấu khăm
Lúc hai, lúc bố khi nằm lắp thêm tư
Photpho nói tới không dư
Nếu ai hỏi mang đến thì ừ rằng năm
Bạn ơi cố gắng học chăm
Bài ca hóa trị trong cả năm vô cùng cần.”
4. Kết luận
Bài viết trên trên đây của công ty chúng tôi nhằm cung cấp thêm những kỹ năng và kiến thức hữu ích về bảng nguyên tố chất hóa học lớp 8. Để gồm một nền tảng bền vững và kiên cố về môn Hóa học, các bạn học sinh nên hiểu với học thuộc gần như hóa trị cùng nguyên tử khối của những nguyên tố thường chạm chán cùng nhóm nguyên tử trên.
Chúc bạn đọc sẽ có được trải nghiệm tuyệt đối khi tham khảo nội dung bài viết này!
=>> các bạn hãy theo dõi con kiến Guru để update bài giảng cùng kiến thức các môn học khác nhé!
Để hoàn toàn có thể học xuất sắc môn Hóa thì vấn đề ghi ghi nhớ bảng hóa trị những nguyên tố hóa học là yêu ước bắt buộc. Đây cũng là kiến thức cơ bạn dạng sẽ theo những em trong suốt quy trình học cung cấp 2, cấp 3 cùng giúp các em giải đúng đắn các bài bác tập liên quan. Sau đó là những kỹ năng và kiến thức về bảng nguyên tố hóa học lớp 8 thường chạm chán và bài ca hóa trị dễ dàng học, dễ dàng nhớ mà lại gdtxdaknong.edu.vn Education muốn chia sẻ đến các em.
Bảng hóa trị một vài nguyên tố hóa học hay gặp
Số proton | Tên Nguyên tố | Ký hiệu hoá học | Nguyên tử khối | Hoá trị |
1 | Hiđro | H | 1 | I |
2 | Heli | He | 4 | |
3 | Liti | Li | 7 | I |
4 | Beri | Be | 9 | II |
5 | Bo | B | 11 | III |
6 | Cacbon | C | 12 | IV, II |
7 | Nitơ | N | 14 | II, III, IV… |
8 | Oxi | O | 16 | II |
9 | Flo | F | 19 | I |
10 | Neon | Ne | 20 | |
11 | Natri | Na | 23 | I |
12 | Magie | Mg | 24 | II |
13 | Nhôm | Al | 27 | III |
14 | Silic | Si | 28 | IV |
15 | Photpho | P | 31 | III, V |
16 | Lưu huỳnh | S | 32 | II, IV, VI |
17 | Clo | Cl | 35,5 | I,… |
18 | Argon | Ar | 39,9 | |
19 | Kali | K | 39 | I |
20 | Canxi | Ca | 40 | II |
24 | Crom | Cr | 52 | II, III |
25 | Mangan | Mn | 55 | II, IV, VII… |
26 | Sắt | Fe | 56 | II, III |
29 | Đồng | Cu | 64 | I, II |
30 | Kẽm | Zn | 65 | II |
35 | Brom | Br | 80 | I… |
47 | Bạc | Ag | 108 | I |
56 | Bari | Ba | 137 | II |
80 | Thuỷ ngân | Hg | 201 | I, II |
82 | Chì | Pb | 207 | II, IV Chú thích: Chữ màu đen: nguyên tố kim loạiChữ màu sắc xanh: thành phần phi kim Chữ màu sắc đỏ: nguyên tố khí hiếm Hóa trị của yếu tố là tổng số liên kết hóa học cơ mà nguyên tử của nguyên tố đó tạo cho trong phân tử. Bảng hóa trị sẽ bao hàm các thông tin quan trọng như thương hiệu nguyên tố, số proton, ký kết hiệu hóa học, nguyên tử khối với hóa trị của yếu tắc đó. đồ vật tự của những nguyên tố vào bảng nguyên tố chất hóa học sẽ được sắp xếp theo số proton tăng dần. Tuy nhiên, những em đề nghị nhớ rằng, các nguyên tố hóa học chưa phải chỉ bao gồm duy tuyệt nhất một hóa trị. Bên cạnh một số nguyên tố có 1 hóa trị như Hidro (I), Liti (I), Beri (II), Bo (III) thì bao hàm nguyên tố có 2 hóa trị như Cacbon (II, IV), Photpho (III, V), Crom (II, III) hoặc nhiều hơn thế 2 như Nitơ (II, III, IV), lưu huỳnh (II, IV, VI) tuyệt Mangan (II, IV, VII),… thăng bằng Hóa học Là Gì? định hướng Cân bởi Hóa học Hóa Lớp 10 Có từng nào nguyên tố hóa học?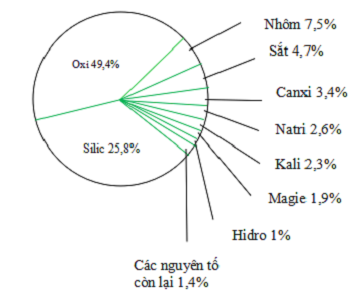 Hiện nay, những nhà kỹ thuật đã tò mò được tổng số 110 yếu tắc hoá học. Vào đó, 98 nguyên tố chất hóa học có bắt đầu từ tự nhiên và thoải mái (trên Trái Đất, khía cạnh trời, mặt trăng…), những nguyên tố còn sót lại là nhân tạo. Bảng hóa trị một số trong những nhóm nguyên tử |
